巯基修饰Oligo还原办法
巯基修饰Oligo的形式
生工生物提供两种形式的巯基修饰形式,分别是裸露的SH和HS-SH,其中SH-Oligo为裸露的巯基,SH-Oligo在运输或者保存过程中能够自发的发生氧化,形成带有二硫键的二聚体结构。而HS-SH-Oligo则是巯基被二硫键保护的形式。
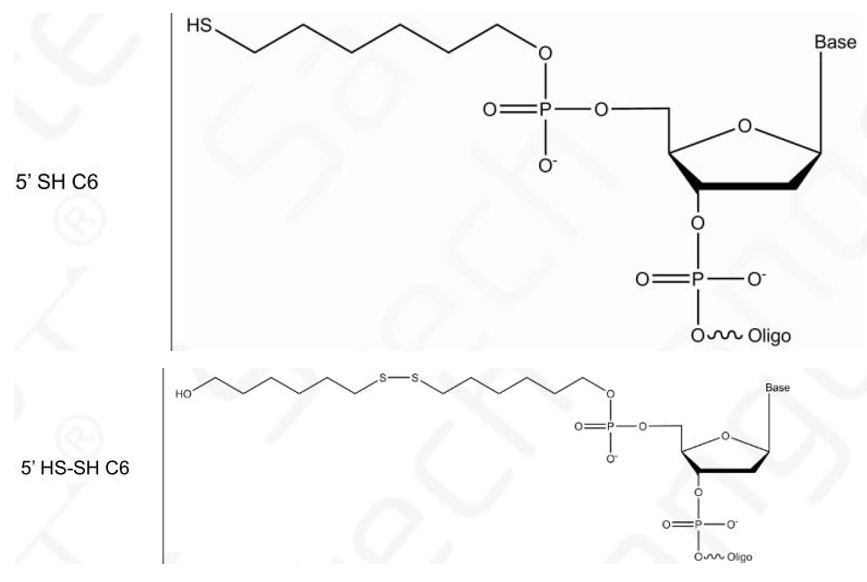
这两类巯基修饰DNA都需要在使用前进行还原处理。还原前后的结构如下图所示:
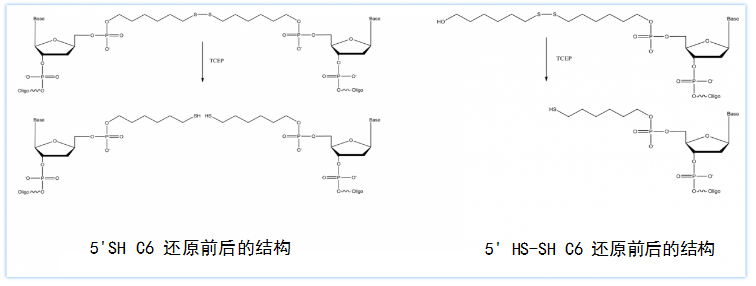
研究化学传感器时,SH-Oligo通常需要先还原成带有裸露巯基的单链,否则其二聚体形式可能会与其他Oligo形成不需要的结构。而HS-SH-Oligo由于始终为单链,因此可以先与其他Oligo形成高级结构之后再进行还原。
另外,HS-SH-Oligo还原之后,会形成与Oligo等量的HO-(CH2)6-SH结构,该结构也带有巯基,会在一定程度上通过竞争来干预SH-Oligo与固相载体的结合。而SH-Oligo从二聚体还原成带有裸露巯基的单链之后,不会产生额外的-SH,不会对SH-Oligo的结合产生竞争作用。
我们推荐使用TCEP(三-(2-甲酰乙基)膦盐酸盐,生工产品编号A600974)作为巯基修饰的DNA使用的还原剂,TCEP粉末可以使用纯水来进行溶解。
巯基修饰Oligo的还原办法
1. 巯基修饰的DNA推荐使用TE缓冲液(10 mmol/L Tris.HCl; 1 mmol/L EDTA,生工产品编号B548106)溶解到100 μM,之后可以根据实验需要稀释到所需要的浓度。
2. 如果用于与金电极相连,将 1 μl 的1 mM TCEP与99 μl的巯基修饰的DNA(浓度为0.2 μM)混合,室温下还原30~60分钟[1],还原之后的DNA可以不去除TCEP用于后续实验。如果需要更高浓度的DNA溶液,比如100 μM,则需要使用10 mM TCEP的进行还原[2]。TCEP物质的量需要在DNA物质的量的100倍或以上。
3. 如果用于与纳米金连接,可将 200 μl 的15 μM的巯基修饰的DNA与 5 μl 的1 M 的TCEP混合,室温下还原30 min。后续可以直接与纳米金溶液混合[3] [4]。
替代的还原剂
DTT(二硫苏糖醇,生工产品编号A100281)也可以用于巯基修饰的DNA的还原,但是因为含有巯基,还原之后必须除去。可以使用DTT溶液(0.1 M DTT,0.18 M PB,PH 8.0)溶解干粉DNA到适宜的浓度,之后葡聚糖凝胶柱(比如NAP-25)进行脱盐处理,去除DTT,之后可以用于后续实验[5]。
注意事项
1.本公司提供的还原办法均参考自相关文献,不保证实际实验效果。
2.TCEP在宽的PH范围(1.5-9.0)均有还原作用,两种还原剂还原后的DNA需要现用现配,不能长时间保存。
3.同时带有亚甲基蓝和巯基修饰的DNA,在还原时溶液颜色可能从蓝色变成无色,此为正常情况,依然可以完成电化学信号的测定,详见参考文献[2]。
参考文献
1. Zhang J, Song S, Wang L, Pan D, Fan C. A gold nanoparticle-based chronocoμlometric DNA sensor for amplified detection of DNA. Nat Protoc. 2007;2(11):2888-95. DOI: 10.1038/nprot.2007.419.
2. Xiao Y, Lai RY, Plaxco KW. Preparation of electrode-immobilized, redox-modified Oligonucleotides for electrochemical DNA and aptamer-based sensing. Nat Protoc. 2007;2(11):2875-80. DOI: 10.1038/nprot.2007.413.
3. Cordray MS, Amdahl M, Richards-Kortum RR. Gold nanoparticle aggregation for quantification of Oligonucleotides: optimization and increased dynamic range. Anal Biochem. 2012 Dec 15;431(2):99-105. DOI: 10.1016/j.ab.2012.09.013.
4. Liu J, Lu Y. Colorimetric Cu2+ detection with a ligation DNAzyme and nanoparticles. Chem Commun (Camb). 2007 Dec 14;(46):4872-4. DOI: 10.1039/B712421J.
5. Hurst SJ, Lytton-Jean AK, Mirkin CA. Maximizing DNA loading on a range of gold nanoparticle sizes. Anal Chem. 2006 Dec 15;78(24):8313-8. DOI: 10.1021/ac0613582.

























 精确搜索
精确搜索 我的草稿
我的草稿
 我的购物车
我的购物车

 精确搜索
精确搜索
